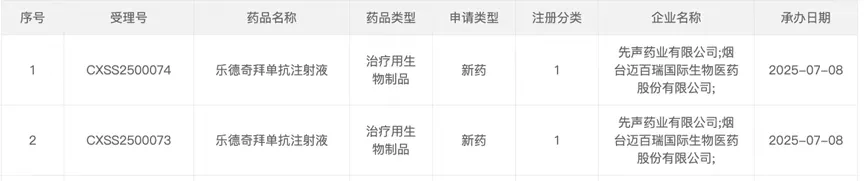
2025年7月8日,先声药业乐德奇拜单抗注射液的上市申请已获受理,推测用于中度至重度特应性皮炎。
关于乐德奇拜单抗
乐德奇拜单抗是一种高效能的抗IL-4Rα单克隆抗体(达必妥同靶点),其阻断由IL-4和IL-13诱导的IL-4Rα信号传导,抑制由IL-4和IL-13诱导的TF-1细胞增殖,具有起效更快、用药频率更低以及更高的临床反应率的潜在临床意义。在许多由Th2细胞介导的疾病中,对IL-4和IL-13的双重抑制被验证为一种有效的治疗策略,例如特应性皮炎、哮喘、慢性鼻窦炎伴鼻息肉、慢性阻塞性肺疾病(COPD)、嗜酸性粒细胞食管炎等。作为下一代IL-4Rα靶点生物制剂,乐德奇拜单抗适用于治疗特应性皮炎和哮喘,具有同类最佳潜力。
特应性皮炎(Atopic Dermatitis,AD)是一种常见的慢性复发性炎症性皮肤病,全球患者人数高达 2.3 亿,在非致命性疾病中疾病负担位居皮肤病之首。
在我国,特应性皮炎患者数量也呈逐年上升趋势。据估计在中国有5000-7000万特应性皮炎患者,它由遗传与环境因素共同作用引发,涉及遗传易感性、皮肤屏障功能障碍、皮肤菌群紊乱及免疫失调等多种发病因素。患者常表现为慢性病程、反复发作,伴有湿疹样皮肤损伤、剧烈瘙痒、皮肤干燥等症状,不同年龄段表现各异。
临床数据
目前三期临床数据尚未披露,公布的II期关键研究中,乐德奇拜单抗显示出了特应性皮炎Q4W治疗的潜力。
在第2阶段,无论第1阶段16周的初始治疗方案如何,达到EASI-50(应答者)的患者将被随机分配至Q2W乐德奇拜单抗组(n=113)或Q4W乐德奇拜单抗组(n=112)。未达到EASI-50(无应答者)的患者则被分配至开放标签Q2W乐德奇拜单抗组(n=86)。
对在第16周达到 IGA 0/1或EASI-75的患者进行的疗效分析显示,采用Q2W和Q4W给药方案,分别有76%-87%的患者在第52周维持了IGA 0/1,92%的患者维持了EASI-75。对所有在第16周使用乐德奇拜单抗达到EASI-50的患者(活性药物反应者)的评估显示,从第16周到第52周,病情持续改善。第52周,达到IGA 0/1的患者增加21%-28%,达到EASI-75的患者增加11%-16%。
临床试验数据表明,患者在使用乐德奇拜单抗后,瘙痒症状迅速得到缓解。首剂用药后短时间内,患者便能感受到瘙痒程度的减轻,并且在持续治疗过程中,瘙痒症状的缓解得以维持,进一步提升了患者的生活舒适度。
在安全性方面,乐德奇拜单抗在临床试验期间展现出良好的安全性特征。整个试验过程中,药物相关的不良反应发生率处于较低水平,且多数不良反应为轻度至中度,患者能够较好地耐受。常见的不良反应如注射部位反应、轻微的上呼吸道感染等,一般不需要特殊处理或仅需简单干预即可缓解,并未导致患者中断治疗,这为药物在临床的广泛应用提供了有力保障。
另外,在对比试验中,与传统治疗手段以及部分已上市的同类靶向药物相比,乐德奇拜单抗在起效速度、临床反应率等方面具有潜在优势。如与一些传统免疫抑制剂相比,乐德奇拜单抗能更快地改善患者症状,缩短患者痛苦的时间;与部分已上市的 IL – 4Rα 单抗相比,乐德奇拜单抗在某些疗效指标上表现更优,有望为患者带来更好的治疗效果。
未来展望
目前针对特应性皮炎的药物非常多,主要集中在生物制剂,JAK口服药,外用药等。 随着越来越多的药物临床逐渐收官,未来特皮可用的药物会越来越多,价格也会逐渐降低。
由于微信最近的功能变动为了保证第一时间收到公众号消息,大家记得把公众号设置为星标。







Leave a Reply