2022年2月24日,中国国家药品监督管理局(NMPA)公示,批准度普利尤单抗注射液,新适应症上市申请,已正式获得批准。
填补国内儿童AD生物治疗领域空白
由于儿童用药的特殊性与传统治疗的局限性,AD患儿病情常常控制欠佳[2]。生物制剂是首个且唯一特异性靶向阻断IL-4和IL-13的免疫调节剂,持续抑制潜在2型炎症[7,8]。生物制剂已分别于2020年6月、2021年9月在我国获批成人、12岁及以上青少年中重度AD适应症,数万中国AD患者使用生物制剂后,瘙痒及皮损快速强效持续改善,生活质量显著改善,并且具有长期临床验证的良好安全性。
此次生物制剂在国内获批6至11岁儿童中重度AD适应症,为更小年龄段的AD患者群体提供了安全、有效的治疗新选择,将改写儿童AD的治疗理念和管理模式,惠及国内广大儿童AD患者。
生物制剂治疗儿童AD安全可靠
LIBERTY AD PEDS研究的安全性结果表明,与安慰剂联合外用糖皮质激素(TCS)相比,生物制剂联合TCS治疗6至11岁儿童重度AD患者的不良事件的总发生率较低;生物制剂联合TCS较常见的不良事件为注射部位反应和结膜炎,这与已知的生物制剂的安全性一致[2,11,12]。
同时,生物制剂实验室安全性结果表明,6至11岁的儿童重度AD患者接受生物制剂联合TCS治疗,常规实验室参数无临床意义变化,提示6至11岁的儿童重度AD患者使用生物制剂不需要进行实验室监测(具体结合临床),这也与青少年、成人中重度AD患者中观察的结果一致[13]。
生物制剂助力儿童AD多维度改善
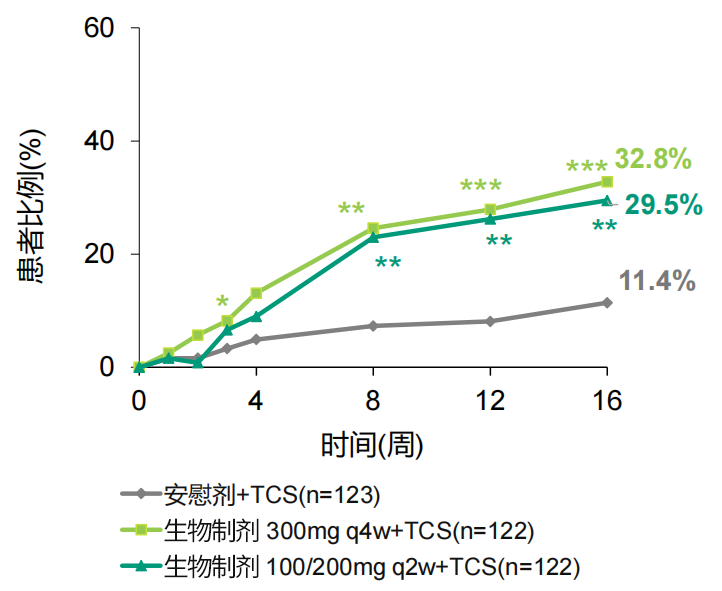
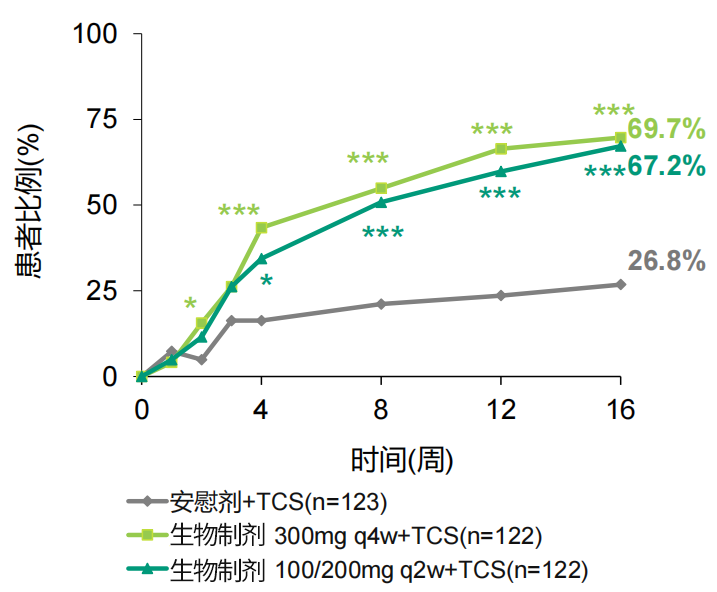
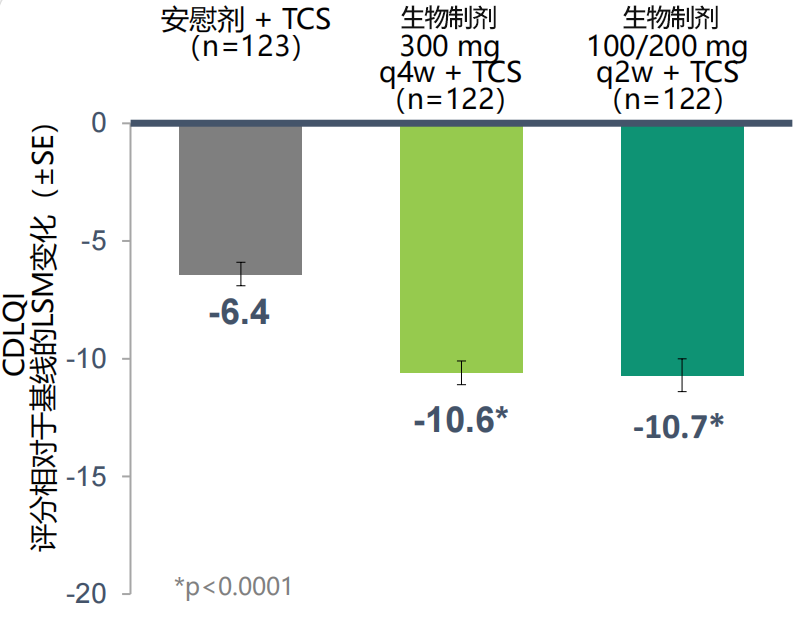
强效清除皮损:生物制剂300mg q4w联合TCS组、生物制剂100/200mg q2w联合TCS组的研究者整体评分法(IGA)0/1应答率分别为32.8%、29.5%,显著高于安慰剂联合TCS组(11.4%)(见图1);生物制剂300mg q4w联合TCS组、生物制剂100/200mg q2w联合TCS组的湿疹面积和严重程度指数评分(EASI)-75应答率分别高达69.7%、67.2%,显著高于安慰剂联合TCS组(26.8%)(见图2)[2,11,12]。
- 中华医学会皮肤性病学分会免疫学组. 中华皮肤科杂志. 2020; 53(02): 81-88.
- Paller AS, et al. J Am Acad Dermatol. 2020; 83(5): 1282-1293.
- Silverberg JI, et al. Ann Allergy Asthma Immunol. 2021; 126(4): 417-428.e2.
- Na CH, et al. Children (Basel). 2019; 6(12): 133.
- Lewis-Jones S. Int J Clin Pract. 2006; 60(8): 984-92.
- Silverberg JI, et al. JAMA Dermatol. 2015; 151(4): 401-9.
- DUPIXENT summary of product characteristics. 2019.
- Guttman-Yassky E, et al. J Allergy Clin Immunol. 2019; 143(1): 155-172.
- 王建琴. 皮肤性病诊疗学杂志. 2020; 27(05): 359-361.
- 孟琳懿, 等. 世界临床药物. 2008; (06): 350-353.
- Paller AS, et al. Presented at: Revolutionizing Atopic Dermatitis Virtual Symposium 2020. April 5, 2020. Oral presentation.
- Sanofi Genzyme and Regeneron. 存档数据[R668-AD-1652].
- Paller AS, et al. Paediatr Drugs. 2021; 23(5): 515-527.
本编号仅作为对本⽂章所涉及的相关药物所属治疗领域科学和临床数据来源真实性的确认,不作为对本⽂章全部内容准 确性、时效性和完整性的确认和保证;本⽂章仅供医疗卫⽣专业⼈⼠为学术交流或了解医学资讯⽬的使⽤,不构成对任何药物或治疗⽅案的 推荐和推⼴。本⽂章所含信息不应代替医疗卫⽣专业⼈⼠提供的医疗建议。



请勿重复进群


加入#中国AD之家#患者微信群


群号:1102465325

Leave a Reply